Lacertilia – jaszczurki
Jaszczurki (Lacertilia dawniej Sauria) → grupa gadów (Reptilia) stanowiąca podrząd w obrębie łuskonośnych (Squamata). Wg klasycznego podziału wydziela się z tej grupy węże (Serpentes), a czasem także amfisbeny (Amphisbaenia), które mają stanowić dwa dodatkowe podrzędy łuskonośnych. Tak definiowane jaszczurki nie są jednak grupą monofiletyczną, a parafiletyczną, dlatego że zarówno amfisbeny, a zwłaszcza węże są silnie wyspecjalizowanymi jaszczurkami. Dodatkowo jak pokazały badania molekularne, amfisbeny są blisko spokrewnione z jaszczurkami właściwymi (Lacertidae). Jednak dla wygody, tutaj węże zostaną pominięte, zaś omówione zostaną „klasyczne” jaszczurki i amfisbeny.
Obecnie opisano ponad 5,5 tysiąca gatunków jaszczurek w tym 181 amfisben. Wyróżnia się 26 rodzin „klasycznych jaszczurek” (lub 37, jeśli Iguanidae uznać za nadrodzinę) oraz 6 rodzin amfisben. Systematyka przedstawia się następująco (na podstawie Vidal i Hedges, 2009 i reptile-database.org):
Domena: Eukarya – eukarionty
Królestwo: Animalia – zwierzęta
Typ: Chordata – strunowce
Podtyp: Vertebrata – kręgowce
Gromada: Reptilia- gady
Podgromada: Lepidosauria – lepidozaury
Rząd: Squamata – łuskonośne
Podrząd: Sauria – jaszczurki
Rodzina: Dibamidae- jaszczurki dwunogie
Infrarząd: GEKOTTA
Rodzina: Pygopodidae
Rodzina: Carphodactylidae
Rodzina: Diplodactylidae
Rodzina: Eublepharidae – eublefarowate
Rodzina: Phyllodactylidae
Rodzina: Gekkonidae – gekonowate
Rodzina: Sphaerodactylidae
Infrarząd: SCINCIFORMATA
Rodzina: Cordylidae – jaszczurki kolczaste
Rodzina: Gerrhosauridae – jaszczurki tarczołuskie
Rodzina: Xantusiidae – jaszczurki nocne
Rodzina: Scincidae – scynkowate
Infrarząd: IGUANIA
Rodzina: Agamidae – agamowate
Rodzina: Chamaeleonidae – kameleony
Rodzina (Nadrodzina): Iguanidae – legwanowate
Infrarząd: ANGUIMORPHA
Rodzina: Shinisauridae
Rodzina: Varanidae – warany
Rodzina: Lanthanotidae
Rodzina: Xenosauridae
Rodzina: Helodermatidae – helodermy
Rodzina: Diploglossidae
Rodzina: Anniellidae
Rodzina: Anguidae – padalcowate
Infrarząd: TEIFORMATA
Rodzina: Gymnophthalmidae
Rodzina: Teiidae – teidy
Infrarząd: LACERTIBAENIA
Rodzina: Lacertidae – jaszczurki właściwe
Rodzina: Amphisbaenidae
Rodzina: Bipedidae
Rodzina: Blanidae
Rodzina: Cadeidae
Rodzina: Rhineuridae
Rodzina: Trogonophiidae
Podrodzina (Rodzina): Corytophanidae
Podrodzina (Rodzina): Crotaphytidae
Podrodzina (Rodzina): Dactyloidae
Podrodzina (Rodzina): Hoplocercidae
Podrodzina (Rodzina): Iguanidae
Podrodzina (Rodzina): Leiocephalidae
Podrodzina (Rodzina): Leiosauridae
Podrodzina (Rodzina): Liolaemidae
Podrodzina (Rodzina): Opluridae
Podrodzina (Rodzina): Phrynosomatidae
Podrodzina (Rodzina): Polychrotidae
Podrodzina (Rodzina): Tropiduridae
Jaszczurki stanowią najbardziej zróżnicowaną grupę wśród obecnie żyjących gadów.
Występują na wszystkich kontynentach poza Antarktyką. Można je spotkać także na wielu wyspach oceanicznych. Zajmują środowiska od pustynnych do tropikalnych lasów deszczowych, od środowisk ciepłych do stosunkowo chłodnych umiarkowanych stref klimatycznych. Osiągają zróżnicowaną wielkość. W tej grupie znajdziemy zarówno najmniejszego owodniowca Sphaerodactylus ariasae (TL= 3cm, SVL= 14-18mm), jak i jednego z największych gadów warana z Komodo (Varanus komodoensis), osiągającego nawet do 3 m całkowitej długości i ok. 50- 70 kg wagi (rzadziej 100- 150 kg). Jaszczurki to zwierzęta naziemne, nadrzewne, podziemne, a także ziemnowodne. Legwan morski (Amblyrhynchus cristatus) jest jedynym gatunkiem żerującym w wodach oceanu. Niektóre jak np. jaszczurki z rodzaju Draco, Ptychozoon, czy Holaspis zdolne są do wykonywania lotów ślizgowych. Większość jaszczurek to drapieżniki. Mniejsze gatunki żywią się głównie bezkręgowcami takimi jak stawonogi, mięczaki czy pierścienice, większe mogą wzbogacać dietę o niewielkie kręgowce. W diecie największych jaszczurek, waranów z Komodo, mogą znaleźć się nawet stosunkowo duże ssaki, takie jak kozy. Wiele drapieżnych jaszczurek wzbogaca swoją dietę o pokarm roślinny, jednak w takim wypadku są to zwykle owoce. Gatunki typowo roślinożerne, u których podstawę diety stanowi pokarm roślinny, głównie w postaci zielonych części roślin, są nieliczne (np. Iguana, Uromastyx, Cyclura, czy Sauromalus).
Przez długi okres czasu sądzono, że istnieją jedynie dwa współczesne, jadowite gatunki jaszczurek tj.: heloderma arizońska (Heloderma suspectum) oraz heloderma meksykańska (Heloderma horridum). Obecnie jednak wiadomo, że jadowite są także niektóre warany (Varanus komodoensis, Varanus varius, Varanus eremius, Varanus indicus) oraz spokrewniony z nimi Lanthanotus borneensis. U wszystkich tych jadowitych gatunków stwierdzono obecność żuchwowych gruczołów „jadowo-śluzowych”. Zarówno helodermy, warany jak i Lanthanotus należą do wydzielonego niedawno kladu Toxicofera (zaliczono tutaj także węże). Przodek tej grupy posiadał zapewne podobne gruczoły, zarówno w żuchwie, jak i w szczęce. Gruczoły takie stwierdzono również u Pogona barbata. Ostatecznie jadowitych gatunków jaszczurek może okazać się więcej, chociaż zapewne u większości z nich uległy one wtórnej utracie jak np. u: Shinisaurus crocodilurus, Xenosauridae, czy Anguidae (choć Pseudopus apodus jest wyjątkiem z zachowanymi gruczołami jadowymi umieszczonymi w szczęce).
Jaszczurki stanowią ważna część ekosystemów. Jako drapieżcy żywią się bezkręgowcami (czasem także kręgowcami) regulując ich liczebność, a z drugiej strony same stanowią pokarm dla innych zwierząt. Roślinożercy biorą udział w rozsiewaniu nasion, a wiec i rozprzestrzenianiu się roślin. Wiele z nich jak np. gekon toke (Gecko gecko) są gatunkami synantropijnymi. W niektórych regionach świata mięso jaszczurek jest cenionym przysmakiem. Zwierzęta te pozyskiwano także dla skór. Jad heloderm, czy zdolności regeneracji ogona wielu jaszczurek są interesujące z punktu widzenia medycyny. Przylgi gekona od lat inspirują badaczy do tworzenia samoprzylepnych materiałów.
Jaszczurki są częścią tradycji i kultury. Z roku na rok stają się coraz bardziej popularne w hodowli i coraz częściej goszczą w naszych domach, obok psów, kotów czy rybek akwariowych. Hodowla gadów to wielki biznes. Wiele osób zarabia na życie rozmnażając i sprzedając egzotyczne gady. Trudno już znaleźć sklep zoologiczny nie posiadający w swojej ofercie choćby jednego gatunku jaszczurki. Cyklicznie organizowane są giełdy terrarrystyczne cieszące się wielkim zainteresowaniem. Część gatunków znajduje się na liście Konwencji Waszyngtońskiej CITES (Convention on International Trade in Endangered Species of Wild Fauna and Flora), która ma za zadanie kontrolować światowy handel zagrożonymi gatunkami. Wiele gatunków jaszczurek jest zagrożonych wyginięciem, głównie przez niszczenie ich siedlisk, a także bezpośrednie odłowy. Międzynarodowa Unia Ochrony Przyrody (International Union for Conservation of Nature, w skrócie IUCN) prowadzi Czerwoną Księgę, w której znajdziemy także wielu przedstawicieli Sauria.
Systematyka jaszczurek oparta na danych morfologicznych
Bazując na danych morfologicznych jaszczurki dzielono na dwie grupy. Podział ten opierał się na sposobie pobierania pokarmu. Pierwsza grupa (Iguania), która zawierała rodziny: Iguanidae, Agamidae i Chamaeleonidae pobiera pokarm za pomocą silnego, mięsistego języka, tak jak w przypadku Sphenodontia (hatterie). Ze względu na podobieństwo do hatterii, klad Iguania uznano za najbardziej prymitywny wśród jaszczurek. Iguania polując polegają głównie na wzroku, a na swoje ofiary czyhają z zasadzki. Druga grupa jaszczurek to Scleroglossa, do którego zaliczano pozostałe rodziny jaszczurek oraz węże. Jaszczurki zaliczane tutaj, posiadają silnie rozwidlony język, który służy im do chemorecepcji i pomaga podczas aktywnego żerowania w poszukiwaniu pożywienia. Pokarm pobierany jest tutaj głównie za pomocą szczęk, z tego też względu uznano tą grupę za bardziej zaawansowaną. W obrębie Scleroglossa wyróżniano: Gekotta (do której zaliczano: Eublepharidae, Diplodactylidae, Pygopodidae, Gekkonidae oraz Sphaerodactylinae), rodziny Dibamidae i Amphisbaenia traktowano jako taksony incertae sedis (o niepewnej pozycji systematycznej), zaś pozostałe zostały zgrupowane w Autarchoglossa. Ta ostatnia grupa zawierała klady Scincomorpha (z: Lacertidae, Teiidae, Gymnophthalmidae, Xantusiidae, Scincidae, Cordylidae oraz Gerrhosauridae) i Anguimorpha do którego prócz Anguidae, Xenosauridae, Helodermatidae, Lanthanotidae i Varanidae, zaliczono Serpentes (węże).
Podział oparty na morfologii został znacząco zmodyfikowany przez badania molekularne.
Systematyka jaszczurek bazująca na badaniach molekularnych
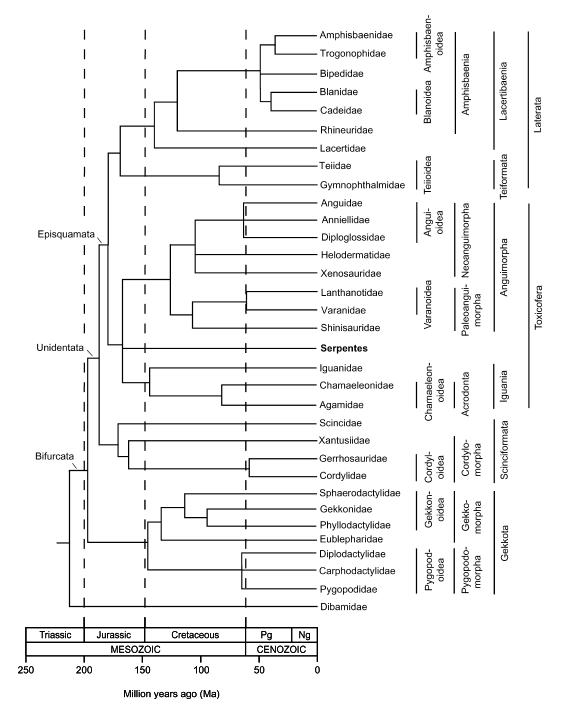
Badania molekularne rzuciły nowe światło na systematykę i filogenezę jaszczurek. Monofiletyczność Iguania została potwierdzona, ale zmieniła się pozycja tej grupy na drzewie filogenetycznym. Klad Scleroglossa stracił rację bytu. Została ustalona pozycja węży, a także ewolucja amfisben, które okazały się blisko spokrewnione z Lacertidae.
Okazało się, że wiele cech morfologicznych potwierdza wyniki badań molekularnych. Najniżej na drzewie filogenetycznym pojawiły się jaszczurki dwunogie (Dibamidae). Wszystkie pozostałe jaszczurki zaliczono do kladu Bifurcata. Cechą morfologiczną odróżniającą tą grupę jest obecność mniej lub bardziej rozwidlonego języka. Monofiletyczność kladu Gekotta została potwierdzona. Jest to grupa będąca drugim bazalnym odgałęzieniem po Dibamidae. Zaliczamy tutaj następujące rodziny: Pygopodidae, Carphodactylidae, Diplodactylidae (wszystkie trzy zaliczane do Pygopodomorpha), oraz: Eublepharidae, Phyllodactylidae, Gekkonidae i Sphaerodactylidae (te cztery rodziny zaliczone do Gekkomorpha). Pozostałe jaszczurki posiadające, w przeciwieństwie do przedstawicieli Gekotta i Dibamidae, jeden ząb jajowy zaliczono do kladu Unidentata.
W obrębie Unidentata możemy wyróżnić dwie grupy: Scincinoformata i Episquamata. Do Scincinoformata zaliczamy następujące rodziny: Cordylidae, Gerrhosauridae, i Xantusiidae (te trzy rodziny zaliczane do Cordylomorpha) oraz najliczniejsza grupę jaszczurek czyli scynkowate (Scincidae). Z kolei Episquamata możemy podzielić na dwie grupy: Toxicofera oraz Laterata. Klad Toxicofera charakteryzuje obecność wydzielających toksyny gruczołów gębowych. Do tej grupy zaliczamy Iguania (Agamidae, Chamaeleonidae, i Iguanidae), węże (Serpentes) oraz Anguimorpha. W obrębie Anguimorpha wyróżniamy klad Paleoanguimorpha (przedstawiciele występujący w Starym Świecie), w którego skład wchodzą: Schinisauridae, warany (Varanidae) i Lanthanotidae (tworzące z waranami grupę Varanoidea) oraz klad Neoanguimorpha (przedstawiciele występujący w Nowym Świecie) z rodzinami: Xenosauridae, Helodarmatidae, Diploglossidae, Anniellidae i Anguidae (trzy ostatnie rodziny zgrupowane w Anguioidea). Warto zauważyć, że węże zostały wyłączone z Anguimorpha, do których były zaliczane wcześniej. Badania molekularne pokazują także, że przystosowanie języka do pobierania pokarmu u Iguania nie jest u nich cechą pierwotną, lecz wtórną, dlatego nie należy umieszczać tej grupy na dole drzewa filogenetycznego. U tej grupy chemorecepcja traci na znaczeniu na rzecz wzroku, jeśli chodzi o wykrywanie pożywienia. Aktywne żerowanie występujące u innych jaszczurek zostaje zastąpione u Iguania polowaniem z zasadzki.
Do Lacerata natomiast zaliczono rodziny: Gymnophtalmidae i Teiidae (obie tworzące klad Teiformata) oraz grupę nazwaną Lacertibaenia do której zaliczamy jaszczurki właściwe (Lacertidae) oraz blisko z nimi spokrewnione amfisbeny (Amphisbaenia). W obliczu takich wyników badań wydzielanie osobnego podrzędu dla amfisben wydaję się pozbawione sensu.
Badania molekularne pokazały, że najbardziej bazalną grupą wśród amfisben nie są przedstawiciele rodziny Bipedidae (1 rodzaj Bipes, który jako jedyny posiada kończyny- tylko przednie), a beznogie Rhineuridae. Dowodzi to temu, że utrata kończyn u amfisben musiała nastąpić trzykrotnie. Okazuje się więc, że utrata lub redukcja kończyn jest dość powszechnym zjawiskiem wśród łuskonośnych.
Dendrogram przedstawiający pokrewieństwo obecnie żyjących grup łuskonośnych, z: N. Vidal, S.B. Hedges, The molecular evolutionary tree of lizards, snakes, and amphisbaenians, C. R. Biologies 332 (2009) 129–139
Dzięki badaniom molekularnym możemy także stwierdzić, że większość występujących dzisiaj jaszczurek wyewoluowało podczas jury i kredy, czyli między 200, a 66 mln lat temu.
Wybrane cechy anatomiczne
Czaszka jaszczurek pochodzi od typu diapsydalnego. Pierwotnie czaszka diapsydalna miała po obu stronach czaszki po dwa doły skroniowe: górny i dolny, oddzielone odpowiednio od spodu, górnym i dolnym łukiem skroniowym. Górny łuk skroniowy zbudowany jest z kości: zaoczodołowej (postorbitale) i łuskowej (squamosum), zaś dolny z kości: jarzmowej (jugale) i kwadratowojarzmowej (quadratojugale). U jaszczurek dolny łuk skroniowy uległ utracie. Dzięki temu uwolniona została kość kwadratowa (quadratum), która tworzy gadzi staw żuchwowy z kością stawową (articulare). Zawieszenie żuchwy na ruchomej kości kwadratowej określa się jako streptostylia. U niektórych jaszczurek, zanika również i górny łuk skroniowy (np. Pygopodidae), co pod tym względem upodabnia je do węży.
Streptostylia sprawia, że czaszka współczesnych jaszczurek jest czaszką kinetyczną (mezokinetyczną). Dodatkowo mogą występować jeszcze dwa punkty ruchomości czaszki: między kością potyliczną (occypitale), a ciemieniową (parietale)- w przypadku większości jaszczurek- lub bardziej z przodu czaszki, między kością ciemieniową, a czołową (frontale)- np. u amfisben. Dzięki temu przednia cześć czaszki może być podnoszona do góry. Jeśli czaszka wygina się w okolicy potylicznej określamy ja jako metakinetyczna, jeśli zaś posiada jednocześnie oba wspomniane wcześniej punkty ruchomości to nazywamy ją amfikinietyczną (Varanus).
To wszystko zwiększa możliwość rozwarcia szczęk, jak i szybkość zamykania oraz otwierania paszczy. Innowacje w budowie czaszki umożliwiły więc chwytanie żywej i ruchliwej zdobyczy przyczyniając się do sukcesu ewolucyjnego tej grupy gadów.
Podniebienie jest mocno podciągnięte pod czaszkę. Wykazuje ruchomość wobec podstawy mózgoczaszki, dzięki obecności stawów pomiędzy kośćmi skrzydłowymi (pterygoideum), a podniebiennoklinowymi (basisphenoideum).
Zęby akrodontyczne lub pleurodontyczne.
Kręgi jaszczurek są przodowklęsłe (proceliczne), za wyjątkiem Gekkonidae i Pygopodidae, u których występują kręgi dwuwklęsłe (amficeliczne). Liczba kręgów szyjnych wynosi zwykle 8, za wyjątkiem kameleonów (3 do 5 kręgów) i waranów (9 kręgów). Liczba kręgów tułowiowych wynosi 16-18, u kameleonów zwykle poniżej 11, zaś większa liczba występuje u wydłużonych jaszczurek beznogich. Najbardziej zróżnicowana pod względem liczby kręgów jest część ogonowa kręgosłupa. Trzony kręgów ogonowych u większości jaszczurek, w części przedniej i tylnej kręgu, przedzielone są tkanką łączną, co ułatwia autotomię ogona (urotomię). Ogon po odrzuceniu z czasem ulega regeneracji, jednak znacznie różni się on od pierwotnego, ponieważ zastępuje go chrzęstny pręt. Mimo łatwości autotomii u amfisben, nie ulega on u nich regeneracji. Jeśli ogon pęka między kręgami, mamy do czynienia z tzw. pseudoautotomią (np. Physignathus).
Żebra jaszczurek są jednogłowe, łączą się z wyrostkami poprzecznymi kręgów. W okolicy piersiowej łączą się z mostkiem. Brak mostka u jaszczurek beznogich. Silnie wydłużone żebra okolicy piersiowej występują u rodzaju Draco. Wystają one poza tułów i stanowią podporę dla błony lotnej. Pozamostkowe żebra u kameleonów, łączą się po stronie brzusznej.
Kończyny zwykle dobrze rozwinięte, pięciopalczaste o formule palcowej 2, 3, 4, 5, 3 lub 4.
W kończynie tylnej obecny jest staw skokowy dolny, który funkcjonuje między proksymalnym, a dystalnym rzędem kości nastopka. Brak tutaj kości ośrodkowych (centrale). Kość odpiszczelowa (tibiale) zrasta się z pośrednią (intermedium) w kość skokową (astragulus). Obecna także kość piętowa (calcaneus) homologiczna z kością odstrzałkową (fibulare).
Niektóre posiadają na palcach przylgi pozwalające zwierzęciu na poruszanie się po płaskich, pionowych powierzchniach (np. Gekkonidae, Polychrotidae). U wielu grup współczesnych jaszczurek doszło do mniejszej lub większej redukcji kończyn (a także samych palców lub tylko ich członów) oraz obręczy barkowej i miednicowej. Beznogie jaszczurki znajdziemy np. wśród: Amphisbaenia, Dibamidae, Pygopodidae, Cordylidae, Scincidae, Anguiodea, czy Gymnophthalmidae. U kameleonów doszło do zygodaktylii (zrośnięcia palców) wskutek czego powstało chwytne autopodium. W przedniej kończynie złączone zostały ze sobą w jedną grupę palce 1, 2 i 3 oraz 4 i 5 tworzące drugą grupę. W kończynie tylnej zaś doszło do zrośnięcia palców 1 i 2, zaś drugą grupę tworzą zrośnięte palce 3, 4 i 5.
Ciało jaszczurek pokrywa zrogowaciały naskórek, a jego wierzchnie warstwy tworzą elastyczne łuski. W niektórych przypadkach są one wzmacniane kostnymi płytkami (osteodermami). Wzór ułożenia łusek na głowie i tułowiu (lepidoza) stanowi ważną cechę systematyczną. Łuski mogą być gładkie lub wręgowane, czasem tworzą większe tarczki, lub przekształcają się w różnego rodzaju wyrostki, rogi kolce czy grzebienie. Inne wytwory skóry mogą tworzyć fałdy lub kołnierze. Struktury te mają wielorakie funkcje. Służą obronie, walce, stanowią część kamuflażu, czy odgrywają rolę w rytuałach godowych.
Pod warstwą rogową znajdują się ciałka zmysłowe (głównie dotyku) posiadające często, sterczące ponad powierzchnię skóry, sztywne pręciki. Szczególnie licznie występują one na głowie.
Generalnie najlepiej rozwiniętymi zmysłami jaszczurek są wzrok oraz zmysł powonienia, który wspomagany jest przez lepiej lub gorzej rozwinięty narząd Jacobsona (przylemieszowy).
W przedniej części twardówki graniczącej z rogówką występuje pierścień składający się z kostnych lub chrzęstnych płytek. Pierścień uczestniczy w akomodacji oka (zapobiega odkształceniu przedniej części twardówki), która polega na zmianie kształtu soczewki. Wokół soczewki występuje dobrze rozwinięty u większości jaszczurek, nabłonkowy pierścień, który przywraca soczewce kształt kulisty. W siatkówce występują czopki pojedyncze i podwójne, zaś u gekonowatych także pręciki. Dodatkowo siatkówka jest wrażliwa na promieniowanie ultrafioletowe. Powieki zwykle są ruchome, rzadziej zrośnięte i przeźroczyste jak u Gekotta. Czasem występuje redukcja oczu jak np. u Dibamidae, czy Amphisbaenia jako przystosowanie do podziemnego trybu życia.
U wszystkich jaszczurek występuje szyszynka, a u większości także nieparzyste oko ciemieniowe (trzecie oko), które u jaszczurek ma postać pęcherzyka. Rolę rogówki odgrywa tutaj przykrywająca oko ciemieniowe, tarczka międzyciemieniowa (interparietalna). Trzecie oko jest narządem fotorecepcyjnym.
Jaszczurki posiadają gruczoły skórne uchodzące poprzez pory preanalne (przedodbytowe) lub femoralne (udowe). Zaś u jaszczurek z rodzaju Tribolonotus (Scincidae) występują unikatowe gruczoły brzuszne i pory dłoniowe. Wydzieliny tych gruczołów pełnią funkcję feromonów.
Narządem wydalniczym jest nerka ostateczna. Głównym produktem przemiany materii jest kwas moczowy z niewielką ilością mocznika.
Układ rozrodczy żeński składa się z parzystych jajników i parzystych jajowodów. W jajowodzie jaszczurek wyróżniamy: odcinek tylny (pochwa), środkowy (długa „macica”) oraz przedni (składający się z lejka i łączącego go z macicą przewodu). Jajniki są groniaste i cienkościenne. Zawierają wewnątrz jamę limfatyczną
Układ rozrodczy męski składa się z parzystych jąder i odchodzących od nich nasieniowodów uchodzących do kloaki. Po bokach otworu kloaki znajdują się dwa hemipenisy stanowiące unikalny i spotykane również u węży- podwójny narząd kopulacyjny.
Rozmnażanie
U jaszczurek jak i u wszystkich gadów zapłodnienie jest wewnętrzne. Narządem kopulacyjnym są wspomniane już wcześniej hemipenisy. Podczas kopulacji zwykle tylko jeden z hemipenisów zostaje wynicowany dzięki wypełnieniu go krwią i limfą. Na powierzchni hemipenisa znajduje się rowek którym spływa sperma. Co ciekawe budowa i ornamentyka hemipenisów stanowią cechę systematyczną.
U większości gatunków witellogeneza i owulacja u samic jest zsynchronizowany z aktywnością jąder u samców. W innym wypadku istnieje możliwość przechowywania nasienia przez samicę. W interakcjach seksualnych i terytorializmie jaszczurek ważną rolę odgrywają sygnały chemiczne. Wydzielina gruczołów skórnych uchodzi poprzez pory preanalne lub femoralne, które są znacznie większe u samców. Kopulacja u wszystkich jaszczurek przebiega bardzo podobnie. Występuje tutaj charakterystyczne gryzienie samicy w kark (co umożliwia przytrzymanie jej w trakcie kopulacji) oraz uniesienie i wygięcie ogona przez samicę. U jaszczurek dominuje poligamia, samiec kopuluje więc z wieloma samicami. Przykładem monogamii mogą być australijskie scynki krótkoogonowe (Tiliqua rugosa).
Wśród jaszczurek możemy wyróżnić:
– jajorodność,
– żyworodność lecytotroficzną,
– żyworodność (prawdziwa placentotrofia).
Jaja z silnie zwapniałą skorupką charakterystyczne są dla gekonowatych (Gekkonidae). Dzięki niej woda jest zatrzymywana w jajach i dlatego mogą być one składane w miejscach stosunkowo suchych np. na pniach drzew, wśród kamieni, czy w budynkach.
Jednak większość jaszczurek składa jaja z elastyczną, pergaminową skorupą. Jaja te podczas inkubacji chłoną wodę z otoczenia i znacznie powiększają swoje rozmiary, nawet do 60 % ich początkowej masy. Jaja te są wrażliwe na wysuszenie, dlatego zwykle składane są w płytkich jamach wykopanych w podłożu, termitierach bądź też w stercie gnijącej roślinności. Miejsca te zapewniają odpowiednio wysoka wilgotność podczas inkubacji.
Jaszczurki z rodzaju Anolis z reguły składają po jednym jaju w krótkich odstępach czasu. Większość gekonów składa na raz po dwa jaja, zaś rekordzistą w ilości jaj jest waran nilowy (Varanus niloticus), który składa nawet do 60 jaj. U brodatki olbrzymiej (Pogona barbata), oba jajniki jednocześnie produkują jaja (witellogeneza w oocytach kolejnego zniesienia rozpoczyna się jeszcze przed zniesieniem jaj z poprzedniego). Wydajność reprodukcyjna tego gatunku jest jedną z największych wśród jaszczurek.
U jajorodnych jaszczurek możemy wyróżnić dwa rodzaje determinacji płci:
– genotypowa (GSD),
– środowiskowa (ESD), dokładniej temperaturowa (TSD– temperature- dependent sex determination).
Temperaturową determinację płci stwierdzono w przypadku nielicznych jaszczurek. Płeć zależy, więc tutaj od temperatury w jakiej inkubowały się jaja. TSD wykryto w rodzinach: agamowatych – Agamidae (np. Agama agama, Chlamydosaurus kingii), eublefarowatych- Eublepharidae (np. Eublepharis macularius), legwanowatych – Iguanidae, jaszczurek właściwych – Lacertidae.
U ok. 30 gatunków jaszczurek stwierdzono zjawisko partenogenezy, w którym komórka jajowa rozwija sie bez obecności plemnika. Potomstwo tych gatunków jest niemal identyczne genetycznie jak osobniki rodzicielskie. Zmienność genetyczna wynika z rekombinacji genetycznej oraz z mutacji. W populacjach tych gatunków brak samców, chociaż występuje tzw. pseudokopulacja, a samica która doświadczyła takiej stymulacji szybciej składa jaja.
Populacje rozmnażające się w ten sposób, bardzo szybko zwiększają swoją liczebność (wszystkie osobniki są samicami, a więc wszystkie składają jaja), jednak wymagają stałego środowiska, ponieważ są mniej plastyczne ewolucyjnie. Zjawisko to opisano u rodzin: Agamidae, Chamaeleonidae, Gymnophthalmidae, Xantusiidae, Gekkonidae .
Zjawisko fakultatywnej partenogenezy zostało opisane przynajmniej u dwóch gatunków waranów: Varanus panoptes i Varanus komodensis kiedy to w ogrodzie zoologicznym w Chester (północna Anglia) uzyskano młode od samicy, która nie miała styczności z samcem.
Ok. 20 % jaszczurek nie składa „klasycznych” jaj, lecz wydaje na świat żywe młode. Jaszczurki te często określa się mianem jajożyworodnych. Dokładniej mamy tu do czynienia z żyworodnością lecytotroficzną, ponieważ większość substancji pokarmowych czerpanych jest przez zarodek z żółtka. Jaja gadów żyworodnych lecytotroficznie nie różnią sie niczym istotnym od jaj gadów jajorodnych. Brak tutaj skorupy jaja, a osłona jajowa jest tutaj cienka i delikatna, co umożliwia jej rozerwanie podczas porodu.
Żyworodność lecytotroficzna w toku ewolucji pojawiła się u jaszczurek przynajmniej 45 razy. Zjawisko to dotyczy 11 rodzin: Agamidae, Anguidae, Chamaeleonidae, Cordylidae, Diplodactylidae, Iguanidae, Lacerdtidae, Scincidae, Trogonophidae, Xsantusiidae, Xsenosauridae. W przypadku krajowych gatunków zarówno jaszczurka żyworodna (Zootoca vivipara) jak i padalec zwyczajny (Anguis fragilis) są żyworodne lecytotroficznie.
U kilku scynków występuje prawdziwa placentotrofia. Przykładem jest ostajnica trójpalczasta (Chalcides chalcides), która posiada łożysko nabłonkowo- kosmówkowe (placenta choriovitellina), które jest jednym z typów łożyska kosmówkowo- omoczniowego i występuje ono również u ssaków nieparzystokopytnych. Wydawanie na świat żywych młodych jest przystosowaniem do życia w chłodniejszym klimacie. Samica wygrzewając się w słońcu zapewnia odpowiednią temperaturę rozwijającym się zarodkom, co w przypadku pozostawienia jaj w gnieździe nie byłoby tak efektywne.
Generalnie nie występuję tutaj opieka nad potomstwem lub jajami. Wyjątki znane są wśród rodziny Scincidae (np. Tribolonotus gracilis, Corucia zebrata, Plestiodon fasciatus czy Plestiodon septentrionalis), Gekkonidae i Varanidae.
Pochodzenie jaszczurek
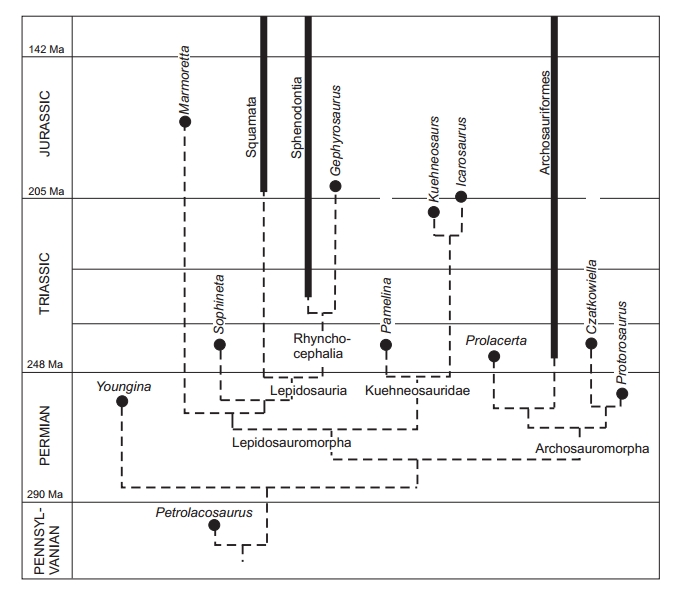
„Prawdziwe” jaszczurki znane są z późnego triasu. Poszukując ich przodka musimy przyjrzeć się jedynym żyjącym dziś przedstawicielom rzędu Sphenodontia (Rhynchocephalia), a mianowicie Sphenodon guntheri i Sphenodon punctatus. Rhynchocephalia są kladem siostrzanym do łuskonośnych. Rozdzielenie tych dwóch grup gadów musiało nastąpić w triasie i najprawdopodobniej było związane ze zmianą sposobu odżywiania się. Przodek obecnych jaszczurek mógł być podobny do obecnych hatterii. Nie można być jednak tego pewnym, choćby dlatego, że obecne hatterie występują w bardzo specyficznym środowisku, do którego zwierzęta te musiały się odpowiednio przystosować. Musimy więc także korzystać z danych paleontologicznych.
Potencjalnymi przodkami jaszczurek (Squamata), jak i Rhynchocephalia mogą być lepidozauromorfy (Lepidosauromorpha) z rodzaju Paliguana lub Saurosternon, występujące w górnym permie i dolnym triasie. Z kolei grupa późnotriasowych, latających (lotem ślizgowym), jaszczurkopodobnych zwierząt należących do Kuehneosauridae była czasem traktowana jako grupa siostrzana dla lepidozaurów (Squamata + Rhynchocephalia). Obecnie dominuje jednak pogląd, że ową grupą siostrzaną jest wczesnotriasowy rodzaj Sophineta, zawierający obecnie tylko jeden znany gatunek, Sophineta cracoviensis, odkryty w Czatkowicach koło Krakowa. W tym ujęciu Sophineta jest najbardziej spokrewniony z lepidozaurami zaś Kuehneosauridae oraz środkowojurajski Marmoretta są dla Lepidosauria grupami zewnętrznymi.
Filogeneza głównych grup gadów diapsydowych z: Evans, S.E. and Borsuk−Białynicka, M. 2009. A small lepidosauromorph reptile from the Early Triassic of Poland. Palaeontologia Polonica 65, 179–202.
Na ewolucję, różnicowanie, a w konsekwencji obecne występowanie jaszczurek ogromny wpływ miał dryf kontynentów, a więc i rozpad Pangei na Laurazję i Gondwanę.
Opracowanie i źródła informacji
Paweł Kaczmarek (jaszczur), na podstawie:
– Sura Piotr, Encyklopedia współczesnych płazów i gadów, Wydawnictwo Fundacja S.C., wyd. I, Nowy Sącz 2005, ISBN 83-88887-60-2
– Pianka Eric, Vitt Laurie, Lizards. Windows to the evolution of diversity, University of California Press, 2003, ISBN 0-520-24847-3
– N. Vidal, S.B. Hedges, The molecular evolutionary tree of lizards, snakes, and amphisbaenians, C. R. Biologies 332 (2009) 129–139
– Evans, S.E. and Borsuk−Białynicka, M. 2009. A small lepidosauromorph reptile from the Early Triassic of Poland. Palaeontologia Polonica 65, 179–202
– Fry, B.G., et al., The structural and functional diversification of the Toxicofera reptile venom system, Toxicon (2012), doi:10.1016/j.toxicon.2012.02.013
– Szarski H. Anatomia porównawcza kręgowców. Wydawnictwo: PWN, Warszawa 1976,
– Hoyer H., Grodziński Z. Anatomia porównawcza kręgowców. PWN, Warszawa 1964
– Dobrowolska Hanna, Zwierzęta świata. Gady, PWN, wyd. II, Warszawa 1990,
ISBN 83-01-08483-9
-Bruins Eugene, Encyklopedia terrarystyki, przeł. Włodzimierz Stanisławski, Galaktyka, Łódź 2003, ISBN 83-87914-76-2
– Attenborough David, Life in Cold Blood, Wielka Brytania, BBC Natural History Unit 2008,
– Ruston W. Hartdegen, Matthew J. Russell, Bruce Young, Richard D. Reams, Vocalization of the crocodile skink, Tribolonotus gracilis (de Rooy, 1909), and evidence of parental care [online], „Contemporary Herpetology” 2001, nr. 2, [dostęp: 08 maja 2011], dostępny w Internecie: http://www.contemporaryherpetology.org/ch/2001/2/
– Li Vigni F., Tribolonotus gracilis. A peculiar „crocodile” in the terrarium, „Reptilia” 2009, nr. 62, str. 57-61
– Jerry G. Wlas, The Guide to Owning Skink,


 [4]
[4]